? IVDR簡介 / Introduction
? 2017年5月5日歐盟體外診斷醫療器械法規(IVDR)正式發布,于2017 年5 月25日正式生效,并于2022 年5 月26 日實施。自實施之日起, IVDR 將取代原歐盟體外診斷設備指令(IVDD)。
? 與大部分國家一樣,歐盟的監管體系也是呈“金字塔” 式的多層級法規體系: 在醫療領域, 法規層級從高到低依次為法規(Regulation)、指令(Directive)、決議(Decision)等,如圖1 所示。
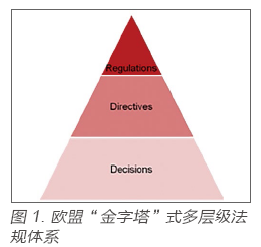
? 本次新發布的IVDR,在法規層級上從原先的Directive(指令)上升為Regulation(法規),標志著歐盟當局對醫療設備領域監管的進一步重視,同時也預示著在歐盟各成員國內醫療器械監管的尺度將得到進一步的統一。
? 分類規則的變化以及公告機構介入的增加:
?在IVDR法規中,對于體外診斷設備的監管依然是基于分類監管這個大框架,但是分類規則較原先的IVDD卻發生了根本性的變化,即在IVDR中,基于產品的風險將所有的體外診斷設備由低到高分為了A、B、C、D四類,如圖2 所示:
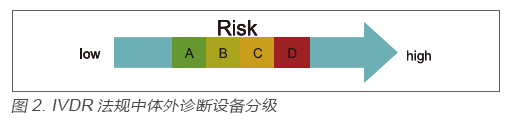
?該分類規則來源于全球協調工作組(GHTF),目前加拿大、巴西、澳大利亞等國已使用,是國際范圍內認可度較高的分類規則。各類產品舉例見表1。

?伴隨著產品分類規則的調整,各類別產品對應的認證途徑自然較原監管體系也有著很大的變化,其中最核心的變化點在于公告機構(Notified Body,NB)介入的增加,涉及產品包括所有的D、C、B類和部分A類。
?在整個IVD領域,涉及公告機構介入的產品數量從IVDD監管體系下的10%~20%增加至80%~90%[2]。告機構介入量的增加,意味著絕大多數的體外診斷設備,在歐盟區的市場準入將要告別原先“自我宣稱”的形式,取而代之的將是一個實質性的注冊過程。
? 歐盟醫療器械數據庫的建立以及監管透明度的增加:
?在歐盟過去十多年的醫療器械監管中,監管的透明度一直是業內詬病比較多的一點。究其原因主要在于沒有一個公開的數據庫供各方查詢[3]。在IVDR的法規體系下,歐盟主管當局一個很重要的工作就是未來將要推出醫療器械數據庫(Eudamed),該數據庫涵蓋從產品上市前審批到上市后監管中的很多重要信息。見圖3:
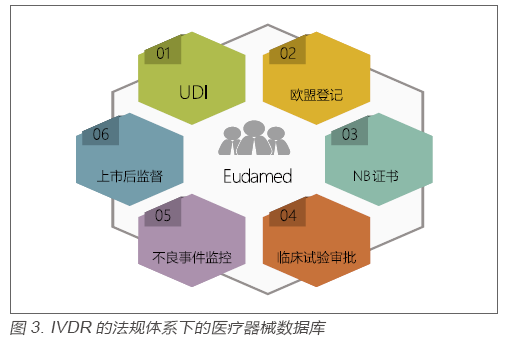
。
?在IVDR中還提出了安全和性能摘要(Summary of Safety and Performance)的要求,以進一步增加監管的透明度。該要求包括C類和D類的產品需要以摘要的形式,將產品規格、性能評估結論及臨床試驗結論等信息公開。通過該摘要,一方面使用者可以更清楚地了解產品的性能指標,另一方面生產企業可以更加詳細地對比同類產品的監管尺度[4]。
? 唯一設備識別系統(Unique Device Identification System, UDI)的引入:
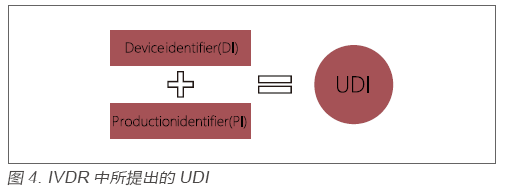
? 繼美國FDA實施UDI的要求以來,世界范圍內紛紛效仿,很多國家相繼推出相關草案。歐盟本次出臺的IVDR,同樣也引入UDI的要求,以增強產品的追溯以及上市后的管理。與FDA的要求一樣,IVDR中所提出的UDI同樣是由一個固定的產品識別碼(Device Identifier,DI)和一個非固定的生產識別碼(Production Identifier,PI)組成,見圖4。生產企業在實施UDI的過程中,需要明確各產品的UDI代碼及所包含的信息,并在產品上加貼UDI標貼,同時以電子形式存儲UDI相關信息并在Eudamed系統上申報。
? 法規負責人的提出:
? IVDR法規中,首次提出了法規負責人的要求:要求每個制造商企業內,至少任命一位法規負責人,負責處理與產品相關的監管、合規性相關工作。具體的職責包括產品批放行、起草和維護CE技術文檔、完成上市后產品的監控、臨床試驗相關文件的簽署等。
?提出法規負責人的要求,標志著新法規IVDR對于執行層面的思考;意味著法規要求在企業內的責任明確、落實到人,從生產企業內部促進著產品的安全性和有效性[5]。
? 過渡期與法規切換:
? 新法規IVDR與IVDD相比變化很大,為避免由于法規切換而造成對現有醫療系統的沖擊,實現法規的“軟著陸”,IVDR法規從生效(Entry into Force)到實施(Application)期間有5年的過渡期。IVDR法規的生效日為2017年5月25日,實施日為2022年5月26日。在生效日前依照舊法規IVDD頒發的CE證書,在證書有效期內持續有效;在生效日后依照舊法規IVDD頒發的CE證書,在實施日后的2 年失效(若證書有效期晚于該時間點)。見圖5。
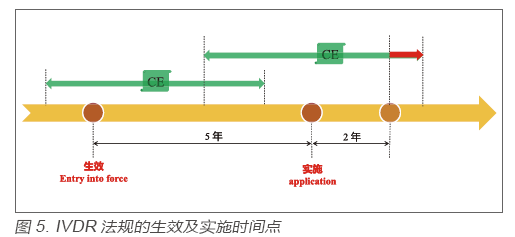
? 所以,在IVDD法規框架下“自我宣稱”類的產品,由于不涉及CE證書,故需要在實施日前完成IVDR法規的切換;少部分在IVDD法規框架下涉及CE證書的產品,需要在證書有效期內完成IVDR法規的切換,但不得晚于實施之后的2 年。
? 后續:
?歐盟區是各醫療器械制造商核心目標市場之一,也是全球第二大的體外診斷設備市場。滿足IVDR法規的要求對各制造商有著不言而喻的巨大作用,各生廠商在未來的幾年內都需要對此開展緊鑼密鼓的法規跟蹤及實施工作。




共有條評論 網友評論